【夏期講習2017】センター化学の勉強を始めよう①
こんにちは。大学受験の理系科目を担当しています、石川です。
何回かに分けて高校(基礎なし)化学についての紹介をします。
来年大学受験を控えている受験生が、この夏に化学は何の勉強をすべきかというと、
・カリキュラムを消化する
・センター試験の対策をする
・入試対策用の問題集を解き始める
のような選択肢が考えられます。 一概に何がいいとは言えませんが、上から順番に優先度が高いです。
つまり、(公立高校ではよくあることですが)まだ学校で全カリキュラムが終えられていないようであれば、
先取りになろうとも、今後の演習時間の確保のために全範囲を早急に終わらせる必要があります。
(化学は特に自分で勉強するのが難しいと思うので、TESTEAなど個別指導塾で自分の学校で終わっていない範囲だけを習うのが効率的です。)
高校化学の全範囲が終わっているなら、次にセンターレベルの問題を解き始めることで、
基本的な問題が解けるようになっているかの確認をし、それもOKな状態なら、
「重要問題集」など入試対策用の問題集を解き始めたほうがいいでしょう。
今回は、夏前までにスタディサプリのような流行りの映像授業で、先取り学習をした生徒さんに対して、
TESTEAの夏期講習でセンター試験対策を始めた例を紹介します。
TESTEAの授業内で問題を解いてもらうことはめったにありません。解説が中心です。
センター対策ならば予めセンター形式の問題集を解いてきてもらって、解説だけで90分使います。
今回は駿台の実践問題集を1回分解いてきてもらいました。
センター1回分の解説に90分??
いえいえ、周辺事項を確認していたら90分でも解説しきれません。
生徒さんの得点力、理解度によってここにかかる時間は変わってきてしまいます。
個人的な目安としては最初の解説はほぼ化学の全範囲の内容確認になるので、
90分×2回~90分×3回は解説に時間を要します。
そこから(復習して覚えるべきことを覚えて)定着が良ければ1回の解説に必要な時間が減衰していきます。
さらに、問題を解いた後に、「ここまで確認する必要があるのか」と気づいてもらえれば、
正しい方法で自分でセンター対策の勉強をできるようになっていきます。
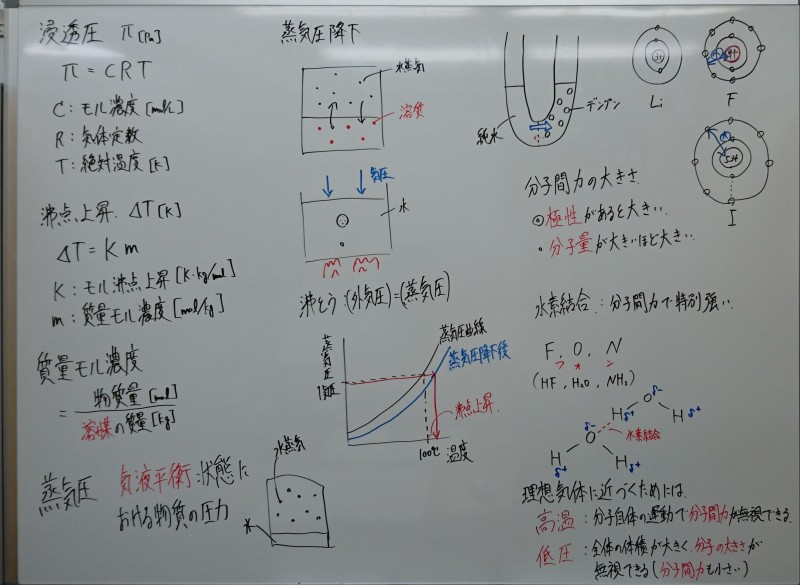
最初の写真はこの解説時の板書ですが、周辺事項でどのような質問をしているかを順々に記載していきます。
実況中継のような感じで読んでいってください。
【浸透圧に関する問題】
Q. 浸透圧を求める公式は?
A. \[ \Pi = CRT \]
\( \Pi \):浸透圧[Pa] \( C \):モル濃度[mol/L] \( R \):気体定数 \( T \):温度[K]
Q. 浸透圧はなぜ発生するの?
A. (問題ではU字管で間に半透膜がある場合で考えています。)
溶媒は半透膜を通過することができるが、不揮発性の溶質は半透膜を通過できない。
溶質が溶媒の動きを妨げるから、溶質が解けている方に溶媒が移動することで液面の差が生じる。
この差を解消するために必要な外圧が浸透圧。
【浸透圧から派生した周辺事項の確認:沸点上昇】
Q. この仕組みって沸点上昇とか凝固点降下とかと同じだよね。沸点上昇度を求める公式は?
A. \[ \Delta T = Km \]
\( \Delta T\):沸点上昇度[K] \( K \):モル沸点上昇[K \( \cdot \) kg/mol] \( m \):質量モル濃度[mol/kg]
Q. この公式の中の「質量モル濃度」はどうやって計算する?
A. $$質量モル濃度\rm{[mol/kg]}=\frac{溶質の物質量\rm{[mol]}}{溶媒の質量\rm{[kg]}}$$
Q. 沸点上昇はなぜ起こる?
A. 純粋な液体ではなく、溶液になると溶質が蒸発を妨げるので蒸気圧降下が発生する。
沸点上昇は蒸気圧降下の結果として発生する。
【沸点上昇から派生した周辺事項の確認:蒸気圧降下】
Q. そもそも蒸気圧とは?
A. 気液平衡状態における物質の圧力のこと。
(気液平衡状態は質問に答えられたのでこれ以上は突っ込まなかったが、
液体→気体への変化の速度と、気体→液体への変化の速度が同じ状態を気液平衡状態という
つまり蒸気圧はその空間に含むことができる気体の最大量と考えることもできる)
Q. 沸騰と蒸気圧の関係は?(富士山の上では水は100℃未満で沸騰するのはなぜ?)
A. まず蒸気圧は温度によって大きくなる。(蒸気圧曲線のグラフを参照)
沸騰は外気圧と蒸気圧が釣り合っているときに発生する、液体の内部から気体に変わる変化のこと。
富士山の上など外気圧が低いところでは、水の沸点が下がる。
ここまで深掘りして確認すると、溶液の性質として「蒸気圧降下」と「沸点上昇」が理屈として繋がるはずです。
断片的な知識ではなく、すべて理屈でつなげる作業。これをTESTEAでは個人個人にあわせて指導していきます。
しかし、解説・周辺事項の確認はここまでやっていても、まだ最初の1問目という。。。
既に理解しているであろう問題は、簡単な質問で流しますが、
「理解していないな」
「理屈が説明できていないな」
と思われる内容についてはかなり突っ込んで確認していきます。
この作業を早めにやっておかないと入試問題には取り組めないので、
センターの問題集など問われている知識の根が浅いものから確認していき、
ゆくゆくは入試問題を解けるように練習していく必要があるのです。
続きはまた後日。。。
☎03-3335-2774
東京都杉並区久我山3-24-18 ティアイビル2階
(受付時間:13時30分~22時 日曜日を除く)
テスティーの2017年合格実績はこちら!